
Lịch sử hình thành và phát triển của ISO 22000
Trong bối cảnh kinh tế ngày càng phát triển, yêu cầu về an toàn thực phẩm ngày càng tăng cao. ISO 22000 trở thành một trong những tiêu chuẩn quan trọng trong ch...
Trong bối cảnh tình hình dịch bệnh Covid-19 ngay ra những hậu quả nghiêm trọng tại khắp nơi trên thế giới, nhu cầu nhập khẩu trang thiết bị y tế nói chung và khẩu trang y tế nói riêng ngày một gia tăng, mở ra cơ hội thúc đẩy sản xuất và phát triển cho các doanh nghiệp sản xuất, kinh doanh khẩu trang y tế. Tuy nhiên để có thể đưa loại hàng hóa này vào những thị trường lớn, cụ thể ở đây là Mỹ thì doanh nghiệp phải đáp ứng rất nhiều tiêu chuẩn và thủ tục, trong đó phải kể tới việc đăng ký FDA cho khẩu trang y tế, khẩu trang kháng khuẩn.

Các Doanh Nghiệp chuyên sản xuất các loại khẩu trang y tế, khẩu trang vải kháng khuẩn và các loại quần áo bảo hộ y tế muốn xuất khảu vào Mỹ thì cần phải xin đăng ký chứng nhận FDA. Đây là việc cung cấp thông tin sản phẩm của doanh nghiệp vào hệ thống FDA Hoa Kì. Được biết FDA là Cục quản lý Thực phẩm và Dược phẩm - cơ quan quản lý thực phẩm và dược phẩm của Hoa Kỳ (tương tự như cơ quan quản lý nhà nước của Việt Nam).
FDA là tên viết tắt của Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ. Đây là cơ quan chịu trách nhiệm chính cho việc bảo vệ quyền và lợi ích sức khỏe cộng đồng bằng các tiêu chuẩn đánh giá, giám sát vệ sinh an toàn, chất lượng cho thực phẩm và dược phẩm lưu hành tại Hoa Kỳ, bao gồm cả sản phẩm nhập khẩu.
Chứng nhận FDA cho khẩu trang y tế, khẩu trang kháng khuẩn là hoạt động kiểm tra các sản phẩm khẩu trang theo những tiêu chuẩn nghiêm ngặt về nhãn mác, thành phần, cấu trúc chức năng do FDA tiến hành nhằm đảm bảo những sản phẩm này có chất lượng đạt chuẩn và không chứa các chất gây hại cho sức khỏe trước khi lưu thông trên thị trường.
Theo thống kê mới nhất tính tới tháng 7/2021, quốc gia chịu ảnh hưởng nghiêm trọng nhất từ đại dịch COVID-19 là Mỹ với 624.603 ca tử vong, trong tổng số 34.926.529 ca nhiễm. Ngày 15/6/2021 ghi nhận một dấu mốc đáng buồn khi số ca tử vong của nước này đã vượt ngưỡng 600.000 người. Dù số ca tử vong hằng ngày ở Mỹ có xu hướng giảm trong những tháng gần đây, song vẫn có hàng trăm người thiệt mạng do đại dịch mỗi ngày.
Tình hình dịch bệnh diễn biến phức tạp, nhu cầu cấp thiết về khẩu trang và các thiết bị y tế tại Mỹ ngày một gia tăng, chất lượng khẩu trang y tế trở thành một trong những vấn đề được quan tâm hàng đầu trong công tác phòng chống dịch bệnh. Thực tế có tới 1,9 triệu khẩu trang 3M giả đã xuất hiện trong 40 bệnh viện ở nhiều bang, khiến giới chức bệnh viện phải cảnh báo nhân viên và loại bỏ số khẩu trang này. Kể từ khi đại dịch COVID-19 bùng phát, đã có hơn 10 triệu chiếc khẩu trang giả bị cơ quan chức năng Mỹ tịch thu. FDA cho biết: “Đã phát hiện ra một số khẩu trang không đáp ứng tiêu chuẩn như mong đợi, khi mà số lượng bụi mịn đi qua khẩu trang nhiều hơn tiêu chuẩn cho phép”. Vì vậy mà việc kiểm soát chất lượng và mức độ an toàn của mặt hàng khẩu trang y tế nhập khẩu vào Mỹ ngày càng trở nên nghiêm ngặt. Và sở hữu chứng nhận FDA là điều kiện tiên quyết để các doanh nghiệp được cấp phép xuất khẩu khẩu trang y tế, khẩu trang kháng khẩu sang thị trường Mỹ.
Tại buổi tọa đàm "Những vấn đề cần lưu ý khi xuất khẩu thiết bị bảo hộ y tế" do Trung tâm Xúc tiến Thương mại và Đầu tư TPHCM (ITPC), Việt Nam được nhận định là một trong những nhà cung cấp hàng đầu về ba mặt hàng khẩu trang, găng tay và trang phục bảo hộ y tế. Trong đó, mặt hàng khẩu trang y tế được quan tâm nhiều nhất do nhu cầu tăng trưởng đột biến từ các thị trường quốc tế với chi phí đầu tư ban đầu thấp.
KNA CERT đăng kí thành công FDA cho Công Ty TNHH Công Nghệ Thiên Đức với phạm vi Thiết bị y tế - Protective Clothes - mask tại Cụm công nghiệp dốc 47, KP. Long Khánh 1, Phường Tam Phước, Thành phố Biên Hoà, Tỉnh Đồng Nai, Việt Nam.
KNA CERT đăng kí thành công FDA cho Công ty TNHH TBVS Y Tế Lê Minh với phạm vi Thiết bị y tế - mask tại KCN Quế Võ, Xã Phương Liễu, Huyện Quế Võ, Tỉnh Bắc Ninh.
Nhìn chung, mặt hàng khẩu trang được chia thành 3 loại nhưng không phải loại khẩu trang nào cũng bắt buộc phải đăng ký FDA khi lưu hành tại Mỹ. Cụ thể, có thể chia khẩu trang thành 3 loại như sau:
1. Khẩu trang vải thông thường
Với những doanh nghiệp sản xuất khẩu trang vải thông thường không phải là thiết bị y tế nên không cần xin số đăng ký với FDA.
2. Khẩu trang vải kháng khuẩn
Theo FDA thì khẩu trang kháng khuẩn không phải là thiết bị y tế, doanh nghiệp nên công bố chỉ là Khẩu trang vải thông thường thì sẽ không phải xin số đăng ký với FDA.
Tuy nhiên nếu công bố là khẩu trang kháng khuẩn thì một số đơn vị nhập khẩu của Mỹ họ vẫn yêu cầu khẩu trang kháng khuẩn cần phải xin số đăng ký với FDA thì mới xuất khẩu được vào Mỹ vì nó có yếu tố kháng khuẩn.
3. Khẩu trang y tế
Khẩu trang y tế là thiết bị y tế bắt buộc phải xin được số đăng ký với FDA thì mới được xuất hàng vào Mỹ, link check số đăng ký FDA khẩu trang y tế tại đường dẫn sau trên website của FDA Hoa Kỳ đối với medical device: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfRL/rl.cfm

ĐỐI TƯỢNG CẦN ĐĂNG KÍ FDA VỚI HÀNG KHẨU TRANG
Hiện nay có 2 đối tượng sản xuất khẩu trang được đăng ký FDA bao gồm:
· Các tổ chức đã và đang sản xuất khẩu trang nhưng chưa được đăng ký với FDA.
· Các tổ chức thuộc nhóm ngành sản xuất khác nay chuyển hướng sản xuất khẩu trang.
Trước bối cảnh dịch bệnh hoành hành, Chính phủ Việt Nam đã có những cơ chế tạo điều kiện cho các doanh nghiệp xuất khẩu khẩu trang, trang thiết bị y tế, sang thị trường nước ngoài. Cụ thể:
FDA phân loại thiết bị y tế dựa trên mức độ rủi ro và mục đích sử dụng của nó. Thông thường, khẩu trang y tế, khẩu trang kháng khuẩn và đồ bảo hộ y tế thuộc diện phải thực hiện thông báo tiếp cận thị trường Premarket 510(k) trước khi nhập khẩu vào Mỹ ít nhất 90 ngày. Tuy nhiên, do tình hình khan hiếm khẩu trang y tế và nhu cầu cấp bách về khẩu trang kháng khuẩn tại Mỹ, Cục quản lý Thực phẩm và Dược phẩm Mỹ đã tạm thời gỡ bỏ một số rào cản liên quan tới thủ tục đăng ký FDA. Cụ thể, FDA cho phép các mặt hàng khẩu trang được phép nộp đơn xin miễn duyệt hồ sơ theo quy trình cũ (quy trình Premarket Approval). Thay vào đó là chương trình khẩn cấp mang tên “Ủy quyền sử dụng khẩn cấp” (EUA – Emegency Use Authorization) với thời gian kiểm duyệt chỉ trong 5-10 ngày cho các doanh nghiệp đáp ứng đủ các điều kiện về thiết kế nhãn mác, tài liệu kỹ thuật, các chứng nhận liên quan… CEO của Super Cargo Service – Công ty dịch vụ hậu cần (logistic) cho biết: “Có doanh nghiệp bị hai quan Mỹ giữ lại hàng tấn khẩu trang vì sản phẩm chứa thông tin “sử dụng cho mục đích y tế” (medical use) nhưng lại không có đủ chứng từ. Do đó, doanh nghiệp cần tránh sai sót này. Cần lưu ý sự thay đổi này chỉ là tạm thời, các thủ tục và quy trình cũ có thể được áp dụng lại bất cư slucs nào, vì vậy đây là “thời điểm vàng” để các doanh nghiệp sản xuất thiết bị y tế tiếp cận thị trường Mỹ nhanh chóng và dễ dàng hơn.
Thông tin cơ bản của doanh nghiệp: Tên công ty, địa chỉ, số điện thoại,…
Hồ sơ pháp lý của doanh nghiệp
Thông tin chung về sản phẩm
Số model sản phẩm
Mẫu bao bì, tem nhãn của sản phẩm
Sản phẩm có được sản xuất theo tiêu chuẩn FDA 21 CFR Part 820 hay ISO 13485: Medical Devices – Quality Management Systems – Requirements for Regulatory Purposes hoặc bất kỳ tiêu chuẩn chất lượng tương đương nào dành cho nhà sản xuất và nhà nhập khẩu
Mô tả các kiểm nghiệm đã được thực hiện trên sản phẩm
Kế hoạch theo dõi, báo cáo và thu hồi sản phẩm trong trường hợp sản phẩm không đạt chất lượng
Mỗi sản phẩm y tế sẽ được phân vào các cấp độ khác nhau. Có tất cả 3 cấp độ (Class):
Sản phẩm khẩu trang y tế thì FDA chỉ phân loại thành 2 nhóm cấp độ 1 và cấp độ 2
CÁC TIÊU CHÍ KIỂM NGHIỆM DÀNH CHO NHÓM SẢN PHẨM KHẨU TRANG THUỘC CẤP ĐỘ 2
Các sản phẩm khẩu trang thuôc nhóm Cấp độ 2 phải trải qua các tiêu chí kiểm nghiệm sau:
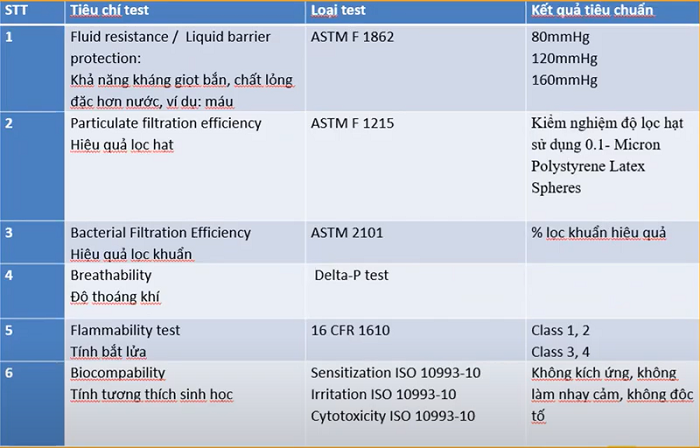
Chi tiết các tiêu chí kiểm nghiệm cho sản phẩm thuộc Cấp độ 2
Có 3 nhóm hồ sơ chính bao gồm:
Bước 1: Cung cấp thông tin
Đơn vị liên hệ với KNA và cung cấp các thông tin cần thiết để được hỗ trợ
Bước 2: Soạn hợp đồng và báo phí dịch vụ đăng kí FDA cho khẩu trang y tế
Căn cứ vào những thông tin mà đơn vị cung cấp, KNA sẽ gửi hợp đồng và báo phí cho doanh nghiệp.
Bước 3: Ký kết hợp đồng
Nếu không có vấn đề gì, đơn vị ký kết vào hợp đồng hợp tác với KNA để hai bên chính thức triển khai hoạt động đăng ký chứng nhận FDA cho sản phẩm khẩu trang y tế, khẩu trang kháng khuẩn
Bước 4: Đào tạo FDA
KNA Cert phổ biến cho doanh nghiệp các thông tin, thủ tục và quy trình cấp giấy phép FDA cho sản phẩm khẩu trang y tế, khẩu trang kháng khuẩn
Bước 5: KNA giúp doanh nghiệp xác định mã sản phẩm và loại hồ sơ cần đăng ký
Với sản phẩm khẩu trang y tế thì FDA chỉ phân loại thành 2 nhóm ở:
Tương ứng với 2 nhóm này sẽ có 2 nhóm hồ sơ khác nhau, các thông tin về bao bì của những nhóm này cũng khác nhau. Vì vậy cần xác định các thông tin này trước khi tiến hàng thiết kế bao bì ở bước 2
Bước 6: KNA hỗ trợ doanh nghiệp thiết kế bao bì theo tiêu chuẩn FDA
Căn cứ vào mã sản phẩm sẽ có các quy định riêng về bao bì việc bao bì cần thể hiện những thông tin gì. KNA kiểm tra bao bì sản phẩm theo tiêu chuẩn của FDA. Trong trường hợp bao bì chưa đạt chuẩn FDA, KNA tiến hàng hỗ trợ cho doanh nghiệp để sửa đổi và khắc phục theo đúng yêu cầu của FDA
Bước 7: KNA hướng dẫn doanh nghiệp đăng ký hồ sơ FDA
Đăng ký hồ sơ tương ứng với nhóm sản phẩm đã xác định:
Bước 8: Hỗ trợ doanh nghiệp lập kế thu hồi sản phẩm lỗi và báo cáo cho FDA
FDA quy định doanh nghiệp có nghĩa vụ khai báo cho FDA khi sản phẩm phải thu hồi khỏi thị trường (adverse event report). KNA sẽ hỗ trợ doanh nghiệp lập hoạch kế hoạch này để hoàn thiện quy trình đăng ký FDA.
KNA CERT đăng kí thành công FDA cho Công ty CP Y tế GICO với phạm vi Thiết bị y tế - mask tại 10/3 Ngách 207/103 Xuân Đỉnh, Xuân Đỉnh, Bắc Từ Liêm, Hà Nội.

KNA CERT đăng kí thành công FDA cho Công ty TNHH VEN SYSTEM với phạm vi Thiết bị y tế - mask tại Đường TS10 Khu Công Nghiệp Tiên Sơn Xã Nội Duệ Huyện Tiên Du Tỉnh Bắc Ninh, Xã Nội Duệ, Huyện Tiên Du, Tỉnh Bắc Ninh.
Ngày 24/4/2020 FDA phát hành bộ luật Ủy quyền sử dụng khẩn cấp (Emergency Use Authorization) cho các nhóm khẩu trang, bao gồm khẩu trang vải không để nhãn là khẩu trang phẫu thuật và không có khả năng kháng giọt bắn (non-surgical mask). FDA cho phép các nhóm khẩu trang này nhập khẩu vào Mỹ mà không cần đăng ký FDA, miễn là doanh nghiệp đạt được các điều kiện về bao bì theo luật EUA (Emergency Use Authorization). Cụ thể, bao bì không được chứa các thông tin sau:
Một số điều kiện khác để sản phẩm khẩu trang được miễn đăng ký chứng nhận FDA khi nhập khẩu vào Mỹ bao gồm:
2: Quy trình để được miễn đăng ký FDA
3: Đặc điểm của phương thức miễn đăng ý FDA
Ưu điểm của phương pháp này:
Nhược điểm của phương pháp này:
